Die periphere arterielle Verschlusskrankheit ist eine chronische Erkrankung mit einer langen Entwicklungszeit. Sie kann Jahrzehnte beschwerdefrei bestehen und ist eine wichtige Indikatorerkrankung für andere kardiovaskuläre Erkrankungen – im Sinne der Spitze eines Eisbergs.
Kommt der Patient mit der Symptomatik einer pAVK in Ihre Praxis, ist sein kardiovaskuläres Risiko bereits deutlich erhöht. Die Mortalität bei pAVK wird vor allem durch die KHK bestimmt.Fünf Jahre nach klinischer Manifestation versterben bei asymptomatischer pAVK 19,1 % und bei symptomatischer 23,9%. Das Risiko eines Schlaganfalls ist zwei- bis dreifach erhöht. Daher ist die Früherkennung der Erkrankung so wichtig, um Risikofaktoren und Begleiterkrankungen rechtzeitig und angemessen behandeln zu können.
Entstehung der pAVK
Die arterielle Verschlusskrankheit entwickelt sich über Jahrzehnte. Wichtigster Risikofaktor ist der Nikotinabusus. Das Alter, ein langjähriger Diabetes mellitus, Fettstoffwechselstörungen und Hypertonie erhöhen das pAVK-Risiko. Für die Adipositas ist allerdings keine Korrelation mit der Wahrscheinlichkeit der Entwicklung einer peripheren arteriellen Verschlusserkrankung belegt. Ein erhöhtes CRP und Fibrinogen sind als Marker von Entzündungen mit einer peripheren arteriellen Verschlusskrankheit assoziiert.
Subintimale Cholesterinablagerungen und Entzündungen der Gefäßwand stehen am Anfang der Krankheitsentwicklung. Der Wanddurchmesser nimmt zuerst zu, das Lumen ist primär nicht betroffen. Dieses Stadium ist symptomfrei.
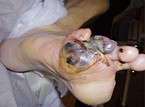
Im Laufe der Zeit entstehen Plaques (Abb. 1), die von umgewandelten Muskelzellen fragil überhäutet werden. Rupturieren diese, können Cholesterinkristalle und angelagerte Thromben in die Peripherie embolisieren. Reparationsvorgänge oder Thromben können das durchströmte Lumen zunehmend einengen. Symptomatische Stenosen und Verschlüsse entwickeln sich. Umgehungskreisläufe können den distalen Perfusionsmangel mindern oder aufheben. Bei einer dilatierenden Arteriopathie bilden sich Aneurysmen.
Anamnese
Die Anamnese allein lässt bereits eine Stadieneinteilung zu. Am gebräuchlichsten ist die Einteilung nach Fontaine, differenzierter die nach Rutherford (vgl. Tabelle 1).
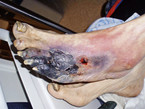
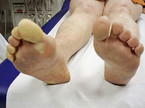
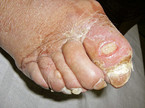
Typische Symptome der pAVK im Stadium der klinischen Erstmanifestation (Stadium II nach Fontaine) sind Schmerzen beim Gehen (Claudicatio intermittens), die meistens eine Etage unterhalb der Region der arteriellen Minderversorgung auftreten. Die Symptomatik akzentuiert sich bei Steigungen oder Erhöhung der Gehgeschwindigkeit. In Ruhe lassen die Beschwerden typischerweise innerhalb weniger Minuten nach. Im Stadium III ist ein Ruheschmerz charakteristisch, der bei Tieflagerung der Extremität gelindert wird. Im Stadium IV entstehen zusätzlich Nekrosen im Bereich der kritischen Mangelperfusion (Abb. 2 und 3).
Zur Beschwerdepalette der chronischen pAVK zählen Kältegefühl, langanhaltende Abblassung nach Anheben der Extremität, trophische Störungen der Haut, Wundheilungsstörung, belastungsabhängiger Schmerz, Muskelkater, Steifheit, Schmerz und Impotenz (vgl. auch Übersicht 1). Beispielsweise verursachen relevante Engstellen im Versorgungsgebiet der Arteria iliaca interna bds. bei Männern Potenzstörungen oder Beschwerden im Bereich der Gesäßmuskulatur (Claudicatio glutealis).
Hämodynamisch relevante Engstellen der Arteria femoralis communis verursachen Beschwerden im Bereich des Ober- und Unterschenkels, der Arteria femoralis profunda im Oberschenkel, der Arteria femoralis superficialis und der Arteria poplitea in den Waden.
Die akute arterielle Verschlusserkrankung ist gekennzeichnet durch schlagartig einsetzende Schmerzen, durch Kälte, Blässe, Gefühlsstörungen, muskuläre Schwäche bis Lähmung, Zelluntergang mit Nekrosenbildung und Schock (Übersicht 2). Sie wird ausgelöst durch lokale Akutthrombosen oder Embolien (kardiogen, aortal, arterioarteriell, paradox), auch von Cholesterinkristallen, spontan oder im Rahmen von interventionellen Eingriffen. Auch nach Katheteruntersuchungen eingebrachte Verschlusssysteme in der Leiste können distal davon lokalisierte Ischämiesyndrome verursachen.
Untersuchung
Klinische Untersuchung (Gefäßstatus)
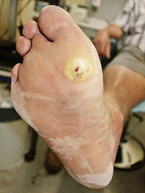
Unser Augenmerk sollte sich auf den Füllungszustand der Venen, purpurrote oder livide Färbung der kühleren Haut, Abblassen bei Hochlagerung der Extremität (Abb. 4), atrophische Störungen der Haut, abhebbare Hautfalten und allgemeine Atrophie der Extremität richten.
Am entkleideten Patienten beurteilt man den Gang mit Hinweisen für eine sensomotorische Neuropathie. Weitere Zeichen sind trockene Haut mit Hyperkeratosen, Hautläsionen im Bereich der druckexponierten Areale, Mykosen und Einblutungen unter die Nägel, Krallen- und Hammerzehen sowie Atrophie der Muskulatur zwischen den Mittelfußknochen. Aus differenzialdiagnostischen Erwägungen ist ein neurologischer Status zum Ausschluss einer Neuropathie (Abb. 5 und 6) zu erheben.
Der Pulsstatus wird erhoben durch Tasten in der Leiste, in der Kniekehle und am Innenknöchel für die Arteria tibialis posterior und am Fußrücken für die Arteria dorsalis pedis. Eine Auskultation in der Leiste lässt Strömungsgeräusche bei Stenosen im Bereich der Arteria femoralis communis, Abgang der Arteria femoralis profunda bzw. der Arteria femoralis superficialis entdecken, am besten bei 70 – 80 %igen Einengungen. Darunter oder darüber kann der Auskultationsbefund negativ sein.
Ein einfacher, in der Praxis leicht anwendbarer Funktionstest ist der Ratschow-Test. Der Patient legt sich auf den Rücken, zieht die Beine rechtwinklig an und hält mit den Händen die Oberschenkel fest. Er kreist dann die Füße mindestens 30- mal bzw. so lange, bis er wegen Schmerz oder Schwäche abbrechen muss. Bei Engstellen werden Unterschenkel und Fußsohle blasser als auf der gesunden oder gesünderen Seite. Jetzt bittet man den Patienten, sich aufzusetzen und die Beine herunterhängen zu lassen. Sie beobachten, dass die blassen Extremitäten hyperämisch werden. Auf der kranken Seite dauert es deutlich länger. Die Haut bleibt anhaltend düsterrot. In der Regel dauert es nur fünf bis acht Sekunden bis zum Wiedereintritt einer Hautrötung und zehn bis zwölf Sekunden bis zur Hautvenenfüllung. Bei gut kollateralisierten Engstellen oder Verschlüssen kann ein Abblassen der Fußsohle fehlen. Der Zeitbedarf bis Beginn des Hauterythems wird für beide Extremitäten per Sekundenzeiger dokumentiert.
Knöchel-Arm-Index
Bei symptomatischen und asymptomatischen Patienten mit Risikoprofil einer peripheren arteriellen Verschlusskrankheit wird der ABI (= Ankle-Brachial-Index/Knöchel-Arm-Index)-Test durchgeführt. Es erfolgt eine herkömmliche RR-Messung an beiden Oberarmen (Kompression der Aa. brachiales) mit der Dopplersonde über der Arteria cubitalis. Malleolär wird mit Hilfe einer Dopplerstiftsonde und einer am Unterschenkel angelegten Blutdruckmanschette ebenfalls gemessen. Die Manschette wird 20 – 30mmHg über den vorher gemessenen systolischen Oberarmdruck aufgepumpt und dann langsam abgelassen. Der Verschlussdruck rechts und links wird dann jeweils über der Arteria tibialis posterior und der Arteria dorsalis pedis bestimmt.
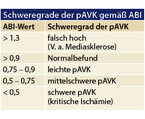
Auf die Durchblutungsreserve kann geschlossen werden, indem der Quotient aus höchstem Verschlussdruckwert am Knöchel je rechts und links und höchstem RR-Wert am Oberarm errechnet wird. Werte ab 0,9 bis 1,3 sind normal, darunter weisen sie auf eine relevante Durchblutungsstörung hin (vgl. Übersicht 3).
Beim Diabetiker können sich wegen einer parallel bestehenden Mediasklerose falsch zu hohe Knöcheldrücke ergeben. Bei Werten über 1,4 ist eine Mediasklerose wahrscheinlich. Falsch hohe Werte ergeben sich auch bei einem peripheren Ödem und bei einer Eingefäßversorgung durch die Arteria fibularis (Fibularisbein).
Weiterführende Untersuchungen
Risikoprofil erheben
Nachdem die periphere arterielle Verschlusskrankheit als Markerkrankheit für Herz-Kreislauferkrankungen gilt, sollten Hypertonie, Koronare Herzerkrankung, Fettstoffwechselstörungen und Diabetes mellitus in Diagnostik und Therapie berücksichtigt werden.
Gehstrecke messen
Zur Objektivierung der schmerzfreien Gehstrecke wird gerne eine standardisierte Belastung vorgenommen. Am einfachsten ist das Abschreiten einer ausgemessenen, ebenen Gehstrecke. Besser ist die jedoch nicht überall verfügbare Gehstreckenermittlung per Laufband. Dabei geht der Proband mit einer Geschwindigkeit von 3 km/h und einem Steigungswinkel von 12 % leicht bergan. Vor und unmittelbar nach dem Belastungstest ist der ABI zu messen. Die symptomfreie Gehstrecke und der Erfolg einer Therapie können mit dem Verfahren objektiver evaluiert werden. Durch Kollateralen kompensierte Stenosen können aufgedeckt werden.
Duplexsonografie
Nach Anamnese, klinischer Untersuchung und ABI-Messung ist bei eingeschränkter Gehstrecke oder/und auffälligem ABI die Methode der Duplexsonografie der nächste diagnostische Schritt. Bei Diabetikern mit sensomotorischer Neuropathie ist die Wahrnehmung der ischämisch induzierten Beschwerden eingeschränkt oder aufgehoben. Mit der Duplexsonografie gelingt eine morphologische Etagendarstellung der Aorta-Becken-Oberschenkel-Unterschenkel-Strombahn und eine exakte Funktionsanalyse von vaskulären Flüssen, Stenosen oder Verschlüssen. Die Methode hat bei guten Untersuchungsbedingungen in der Hand Geübter eine hohe Sensitivität von 88 % und eine Spezifität von 96 % für Stenosen über 50% und Verschlüsse. Sollte keine ausreichende Untersucherexpertise verfügbar oder die Klärung der Gefäßsituation nicht möglich sein, werden die anderen Untersuchungsverfahren (MRT, DSA, Angio-CT) genutzt.
Weitere bildgebende Diagnostik
Bei komplexen Verhältnissen ermöglicht die Angio-MRT eine aussagekräftige Übersichtsdarstellung der arteriellen Strombahn. Eine Niereninsuffizienz (GFR < 30 ml/min/1,73 m²) oder Dialysepflicht schränkt die Gabe von ionischem linearem Chelat Gadodiamid wegen der Gefahr einer nephrogenen Fibrosklerose ein. Hier ist auf dem Einsatz von makrozyklischem Kontrastmittel zu bestehen. Für Stenosen über 50 % oder Verschlüsse liegt die Sensitivität bei 95 % und die Spezifität bei 97 %. Bei Gefäßwandverkalkungen können allerdings Stenosen überschätzt werden. Ein guter Überblick über die Gefäßregionen erleichtert die Planung von Intervention und Operation.
Gezielte Fragestellungen werden mit einer digitalen Subtraktionsangiografie (DSA) beantwortet. Bei beabsichtigter Röntgenkontrastmittelgabe ist eine Niereninsuffizienz oder hyperthyreote Stoffwechselstörung auszuschließen. Bei Diabetikern sind Metformin und Sulfonylharnstoffe 24 Stunden vor der Untersuchung abzusetzen. Auf eine Gabe von nichtsteroidalen Antirheumatika und von Diuretika (soweit möglich) sollte am Tag der Untersuchung verzichtet werden. Eine Antikoagulation ist für den Eingriff auszusetzen.
Eine bildgebende Diagnostik wird immer dann durchgeführt, wenn eine therapeutische Maßnahme – ob interventionell oder chirurgisch – indiziert und zumutbar ist.
Differenzialdiagnose
Die ischämische Symptomatik (Schmerz, Krampf) lässt nach Beendigung der auslösenden körperlichen Belastung in der Regel schnell nach. Sie ist bei ähnlicher Belastung meistens reproduzierbar. Bei fortgeschrittenem Krankheitsstadium (Stadium III und IV nach Fontaine) ist der Schmerz bei Herabhängen der Extremität zumindest geringer als bei Hochlagerung.
Nicht immer ist aus dem Beschwerdebild die Abgrenzung klar und einfach. Wichtige differenzialdiagnostische Erwägungen ergeben sich aus der Lokalisation, der induzierenden Tätigkeit, der Dauer und der Intensität der Belastung.
Spinale Erkrankungen sind eher positions- als belastungsabhängig, können aber eine Claudicatio nachahmen. Sie bessern sich meist nicht durch Ruhigstellung. Mononeuritiden verhalten sich ähnlich. Es besteht ein Dauerschmerz. Zur Bestätigung ist eine differenzierte neurologische Untersuchung, oft mit NMR der Wirbelsäule und des Spinalkanals nötig. Spinalkanalstenosen verursachen oft beidseitige Schmerzen und Schwäche. Eine Linderung der Beschwerden durch Bücken nach vorne kann verzögert eintreten.
Nervenwurzelkompressionen strahlen meist in das gesamte Bein ein und haben einen eher akzentuierten Charakter. Sie werden ausgelöst durch Sitzen, Stehen oder Gehen, sind aber auch oft in Ruhe existent. Ein Haltungswechsel kann die Symptomatik bessern.
Beim Morbus Morton findet sich ein lokaler Druckschmerz im Fußgewölbe, wenn das schmerzverursachende Neurom im Bereich der Fußsohle komprimiert wird. Die Diagnose kann durch ein MRT gesichert werden.
Arthrosen induzieren bei Belastung des betroffenen Gelenks Schmerzen. Bakerzysten sind Folge der arthrotischen Degeneration und führen zu Schwellungen, rupturbedingten Spannungsgefühlen und Ödem. Die kombinierte Absicherung der Diagnose erfolgt durch Sonografie, Röntgen des Gelenks, MRT oder CT. Eine Arthritis verursacht Beschwerden auch unter Belastung. Sie kann akut meistens mit Überwärmung und Rötung auftreten. Der Schmerz lässt sich nicht immer nur auf ein Gelenk projizieren.
Einblutungen in die Weichteile der Extremität beginnen meist mit einem akuten Schmerz („Riss“). Nicht selten begünstigt eine Antiaggregation oder eine Antikoagulation die Blutung. Einfach ist dies durch Anamnese, Sonografie +/- CT zu klären.
Die Claudicatio venosa entsteht bei schwerer Varikosis und Insuffizienz der tiefen Leitvenen, zum Beispiel nach einer tiefen Beinvenenthrombose. Die Beschwerden sind durch schneidende Schmerzen oder Engegefühl charakterisiert. Sie treten unter körperlicher Belastung auf. Der Abstrom bei vermehrter arterieller Perfusion ist gestört. Ruhe und Hochlagerung der Extremität bringen schnelle Entlastung.
Thrombosen, insbesondere Unterschenkelvenen- oder Muskelvenenthrombosen, können auch ohne eine Schwellung der Extremität Schmerzen hervorrufen. Pedalvenenthrombosen sind wegen des plantaren Druck- und Stehschmerzes differenzialdiagnostisch von einem M. Morton abzugrenzen. Die Duplexsonografie in erfahrener Hand klärt die Fragestellung.
Eine Thrombophlebitis ist schnell, leicht und sicher klinisch und durch die Ultraschalluntersuchung mit hochauflösenden Schallköpfen (12 MHz) zu erkennen. Eine adäquate Antikoagulation (mindestens sechs Wochen) ist mit dem Patienten zu besprechen.
Beim Entrapment-Phänomen stellen sich die Beschwerden unter Belastung im Bereich der Wade ein. Das Kompressionssyndrom entwickelt sich vornehmlich bei jungen Menschen, die sportlich aktiv sind. Die Arteria poplitea wird dabei durch anatomische Strukturen (Membranen, Ligamente) oder meist hypertrophierte Muskelzüge unter Anspannung eingeengt. Oft tritt das Syndrom beidseits auf. Klarheit bringt eine Duplex/Doppler-Untersuchung in der Provokationsstellung. Ergänzend wird eine CT durchgeführt.
Die zystische Adventitiadegeneration führt zur Einengung meistens der arteriellen Strombahn durch murale, der Synovia ähnliche, flüssigkeitsgefüllte kleine Hohlräume. Sie kann mit der Duplexsonografie morphologisch sicher erkannt, in der funktionellen Auswirkung bewertet und durch CT bestätigt werden.
Embolien von Cholesterin und/oder Thromben führen zu akut einsetzenden Beschwerden. Sie verursachen vornehmlich akrale Durchblutungsstörungen bis hin zur Nekrosenbildung. Klinisch imponieren sie als Blue-Toe-Syndrom (Abb. 7) oder akrale blitzfigurenartige livide Zeichnung.
Stadiengerechte Therapie der pAVK
Therapie der Risikofaktoren
Als Basisziele in der Behandlung der pAVK sind in der S3-Leitlinie definiert: Progressionshemmung, Risikoreduktion und Reduktion der kardio- und zerebrovaskulären Ereignisse, Besserung der Lebensqualität. In jeder Phase der Erkrankung können diese Ziele unterschiedliche Wertigkeit besitzen.
Die Therapie der assoziierten Risikofaktoren beeinflusst wesentlich die Gesamtprognose der Menschen mit peripherer arterieller Verschlusskrankheit.
In jedem Stadium der Erkrankung sollte das Rauchen eingestellt werden. Die kardiovaskuläre Morbidität und Mortalität wird dadurch vermindert. Eine Unterstützung durch Raucherentwöhnungsprogramme ist bei Bereitschaft des Patienten sinnvoll.
Die Behandlung erhöhter Blutfettwerte (LDL) mit Statinen führt zu einer Reduktion der Gesamtsterblichkeit, zu einer Reduktion der Inzidenz der Claudicatio intermittens und bei mindestens einjähriger Therapie zu einer Verlängerung der Gehstrecke . Die LDL-Werte sollten < 100 mg/dl betragen.
Eine HbA1c-Steigerung um 1 % erhöht das Risiko des Auftretens einer symptomatischen pAVK um 28 %. Von einer optimierten Diabetesstoffwechseleinstellung (HbA1c < 7 %) profitieren die Betroffenen.
Der Zielblutdruck bei Therapie der Hypertonie liegt bei < 140/90 mmHg. Die Behandlung einer Hypertonie mit ACE-Hemmern senkt die kardiovaskuläre Mortalität und kann durch Verbesserung der kardialen Auswurfleistung zu einer Verlängerung der maximalen Gehstrecke führen. Beim Diabetiker führt diese Therapie nachgewiesenermaßen zu einer deutlichen Reduktion der Insultrate (UKPDS).
Die Plättchenaggregationshemmung (Acetylsalicylsäure, Clopidogrel) führt zu einer 54 %igen Reduktion notwendiger peripherer Revaskularisationen.
Stadiengerechte Therapie der arteriellen Verschlusskrankheit
Im Stadium I nach Fontaine bestehen keine Beschwerden. Zufällig oder im Rahmen einer Routineuntersuchung wird die arterielle Verschlusserkrankung erkannt. Thrombozytenaggregationshemmer haben nach den aktuellen Leitlinien keine evidenzgesicherte Indikation, es sei denn, sie werden aus kardiovaskulärer Indikation verordnet. Wichtige Maßnahmen sind Nikotinkarenz, medikamentöse Einstellung einer Hypertonie, des Diabetes mellitus und einer Fettstoffwechselstörung.
Ein Gehtraining ist im Stadium I und im Stadium II sinnvoll. Es sollte im Rahmen eines strukturierten und überwachten Programms unter Aufsicht und regelmäßiger Anleitung erfolgen. Es werden Übungseinheiten von 30 bis 60 Minuten mindestens dreimal je Woche über mindestens drei Monate empfohlen.
Im Stadium II nach Fontaine ist Symptomreduktion das Therapieziel. Gehtraining ist effektiver als eine medikamentöse Therapie und sollte daher vor vasoaktiven Substanzen verordnet werden. Cilostazol ist beispielsweise eine Substanz mit nachgewiesener Gehstreckenverlängerung. Nebenwirkungen und Kontraindikationen wie Nieren- und Herzinsuffizienz sollten vor Verordnung von Cilostazol ausgeschlossen sein.
Acetylsalicylsäure sollte im Stadium II im Rahmen der Sekundärprävention eingesetzt werden.
Je nach Einschränkung der Lebensqualität, Wille des Patienten und Versagen der bisher geschilderten therapeutischen Ansätze ist eine interventionelle Maßnahme zu diskutieren.
Im Stadium III nach Fontaine ist vorrangiges Behandlungsziel der Extremitätenerhalt. Gefäßrekonstruktive Maßnahmen stehen im Vordergrund. Können diese nicht umgesetzt werden, kann eine Therapie mit Prostaglandinen parenteral eingeleitet werden.
Im Stadium IV nach Fontaine ist die Amputation oft unausweichlich. Die diagnostischen Maßnahmen dienen dann der Festlegung der günstigsten Amputationszone und der Sicherung der Operationsfähigkeit. Bei feuchter Gangrän droht eine Sepsis.
Zusammenfassung
Die periphere arterielle Verschlusskrankheit schränkt die Lebenserwartung und die Lebensqualität der Betroffenen deutlich ein. Die Früherkennung ist deshalb von enormer prognostischer Bedeutung und vom Zusammenspiel der gefäßmedizinischen Disziplinen abhängig. In die hausärztliche Kompetenz fällt die Führungsaufgabe in der Basis-Diagnostik der pAVK und die verantwortliche, ökonomische Koordinierung der Spezialisten. Die stadienadaptierte Behandlung der arteriellen Verschlusskrankheit ist generell immer im Kontext der Begleiterkrankungen zu sehen.▪